李 天舒 早稲田大学 理工学術院総合研究所 次席研究員(研究員講師)
研究背景
化学薬品は通常親水性であるため、細胞取り込み率が低いです。さらに、代謝酵素によって容易に分解または非活性化され、血液循環系において不安定です。一方、これらの小分子は全身に分布し、正常組織に望ましくない毒性をもたらす可能性が高いです。そのため、治療効果を改善し副作用を減らすためには高度なキャリア設計が必要です。
リポソームなどのナノ粒子は薬物運搬体として研究または応用されています。薬物を担持し細胞取り込みを増加させる、薬物を代謝酵素から保護する、または特定の組織へ運ぶことを期待されています。脂質の化学構造、組成、ナノ製剤、および表面修飾は、ナノ粒子の特性を決定する重要な因子であり、生物活性プロファイルにも影響を与えます。従って、これらの要因と薬効の関連性はナノキャリア設計の理論的根拠になります。
研究結果
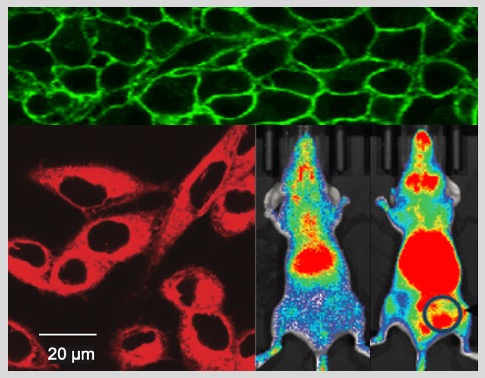
抗がん剤ドキソルビシンの薬効を増加するためにマレイミド修飾されたpH応答性リポソームを作製しました。リポソーム表面のマレイミド部分は細胞表面の遊離チオールとの相互作用により、従来のエンドサイトーシス経路と別に新たなルートで細胞内在化を促進しました。さらに、マウスモデルで皮下注射後腫瘍部位でのリポソームの蓄積を強化し、in vivo治療効果を増強しました。リポソームの主成分はpH応答性を持つため、エンドサイトーシスを経由しエンドソームと呼ばれる酸性の細胞小器官に入った後、薬物がより容易に放出されました。一方、正常組織への毒性を抑制するために、リポソームの表面に一部のヒト乳がん細胞に過剰発現しているErbB2分子を認識する抗体を結合しました。これにより、標的腫瘍への抗がん剤送達を増加させました。一方で、リポソームの肝臓と脾臓での蓄積が増加したことから、単核貪食細胞系(MPS)がこれを除去することで自然免疫系が作動することが懸念されました。
リポソームの化学構造や物理的特性はどのように免疫細胞を影響するかについて、ヒトおよびマウスのマクロファージを用いて調べました。一部のカチオン性リポソームはエンドサイトーシスされた後、リソソーム破裂を誘発し、NLRP3インフラマソームを活性化しました。興味深いことに、あるタイプのリポソームはエンドサイトーシス経路の代わりに細胞膜との融合によって、更なる強力なインフラマソーム活性化を引き起こし、免疫刺激の新しい経路を示唆しました。さらに、これらのリポソームは免疫アジュバントとして働き、モデル抗原であるアルブミンをマウス樹状細胞に効率的に取り込ませました。In vitro実験では、CD8 +およびCD4 + T細胞がともに活性化され、主要組織適合遺伝子複合体(MHC)IおよびMHC IIを介した抗原提示が促進されたことが分かりました。
社会へのインパクト
化学療法は最も使用される抗がん方法ですが、副作用が伴い、患者さんに苦痛を与えます。腫瘍特異的リガンドや多機能脂質を利用し先進なナノメディシンを創り出して、癌患者の痛みを和らげ、生活の質を改善することが期待されています。大量製造プロセスの難しさと高コストのため、現在市場に出回っているリポソーム薬は僅かです。従って、よりシンプルなリポソーム修飾を提案し、薬物ナノキャリアを設計するための新しい方法を示しました。
今後の展望
ナノ粒子は全身投与後にMPSに蓄積する傾向があるため、免疫学的特性を調べて、それらの薬理学的効果を包括的に理解することが必要です。他方、免疫刺激成分または脂質からなるリポソームは、抗原を細胞に送達しながら免疫系を刺激する特徴があるため、アジュバントとしてワクチン開発に貢献することが期待されます。特に、一部のカチオン性脂質は、核酸を高効率で担持することが可能であり、新型mRNAワクチンなどにも適用されると考えます。