反町優理子 早稲田大学生命医科学専攻合田研究室博士1年/国立国際医療研究センター生体恒常性プロジェクト研究生
研究背景
全身性エリテマトーデスは国内だけでも7万人超の患者が存在する難治性の自己免疫疾患で、全身性の炎症反応により生活の質(QOL)の低下をきたします。ステロイドをはじめとする免疫抑制剤が第一選択薬となりますが、ステロイドの長期服用がもたらす副作用は深刻な問題であり、アンメットニーズが高い疾患です。
Solute carrier family 15 member 4 (SLC15A4)は、免疫細胞のエンドリソソーム膜に局在するプロトン共役型アミノ酸トランスポーターで、エンドリソソームの酸性化に伴い、内腔から細胞質へアミノ酸やオリゴペプチドを輸送します。SLC15A4は全身性エリテマトーデスや2型糖尿病の疾患関連遺伝子で、病原体や死細胞に由来する核酸を認識するToll様受容体(TLR)7およびTLR9による炎症シグナルを媒介することで、全身性エリテマトーデスや腸炎の自己免疫疾患の病態形成を担っています。そのためこのトランスポーターは自己免疫疾患の有望な治療標的と考えられています。
SLC15A4がどのように炎症シグナルを制御するかというメカニズムについては、一部は明らかになりつつあるものの、まだ不明な点が多く残されています。SLC15A4を治療標的として新しい自己免疫疾患治療法を開発していくうえで、SLC15A4による炎症制御機構の詳細を明らかにしていくことが極めて重要です。
研究結果
SLC15A4による炎症制御の分子機序を調べるため、近位依存性ビオチン標識法によってSLC15A4と相互作用する可能性のある分子を網羅的に探索し、グルコース代謝に関わる複数分子を同定しました。そこでSLC15A4の発現を低下させたヒト樹状細胞株とSLC15A4欠損マウスマクロファージを用いてグルコース代謝を調べた結果、これらの細胞では、解糖系活性およびミトコンドリア呼吸能が低下していること、ピルビン酸をミトコンドリアへ効率的に受け渡すことができないこと、TCA回路でのグルコース利用の低下を補うためにグルタミンの利用効率を上げていることが分かりました。さらにSLC15A4がピルビン酸脱水素酵素(ピルビン酸をアセチルCoAに変換する酵素)の活性制御に必須であることも明らかになりました。
細菌感染によって活性化されたマクロファージが炎症性サイトカインを産生するためには、解糖系優位に代謝を変化させることが必要です。SLC15A4を欠損すると、感染刺激に依存した代謝変化がマクロファージで正常に起こらないために炎症性サイトカインの産生が低下しました。さらにSLC15A4欠損マクロファージで亢進したグルタミン代謝を抑制すると、炎症性サイトカインの回復が認められました。これは、SLC15A4によるグルコースとグルタミンの代謝バランスの調節が、マクロファージによるサイトカイン産生に重要であることを示しています。さらに私たちは、SLC15A4が細胞外の栄養環境の変化に対して代謝恒常性の維持に必須の役割を果たしていることも明らかにしました。
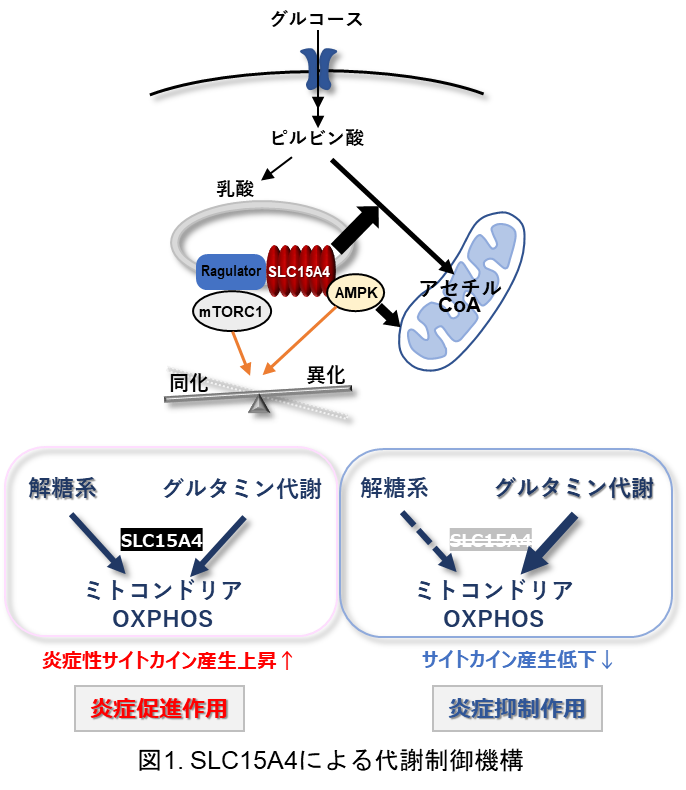
樹状細胞やマクロファージは、炎症が起きた組織で免疫応答を支えている細胞ですが、本研究によって、栄養状態が悪化する炎症部位においてこれらの細胞が機能を発揮するためには、SLC15A4による代謝制御が極めて重要であることが明らかになりました(図1)。
本研究は、国立国際医療研究センター分子炎症制御プロジェクト、慶應大学、理化学研究所、東北大学との共同研究によって得られた成果です。
社会へのインパクト
今回の研究は、SLC15A4が自然免疫細胞の代謝恒常性と炎症時の代謝適応に極めて重要な役割を果たしていることを見いだしたことで、新しい炎症制御機構が明らかになりました。同時に、一見関係がないように見えるエンドリソソームと代謝の基本システムが密接に関連していることがわかりました。さらに、SLC15A4が免疫細胞に選択的に発現していることと今回得られた結果を考え合わせると、解糖系とTCA回路という細胞のエネルギー代謝の根幹を担う生体反応が、細胞種ごとに異なる制御を受けているという興味深い事実も明らかになりました。こうした細胞特異的な制御機構は、副作用が少ない安全域の広い創薬標的となるため、SLEをはじめとする炎症性疾患においてSLC15A4が優れた治療標的であることが今回改めて示されました。マクロファージと樹状細胞は、免疫応答の司令塔として様々な疾患の病態形成を担う細胞です。これらの細胞においてSLC15A4の働きを阻害することで、効果的な炎症抑制効果が得られることが期待でき、今後全身性エリテマトーデスをはじめとする自己免疫疾患の新しい治療法開発に大いに役に立つ成果と言えます。
今後の展望
今回の研究により、マクロファージと樹状細胞の新しい代謝制御機構が明らかになりました。SLC15A4は自己免疫疾患の優れた治療標的ですが、マクロファージと樹状細胞は様々な疾患における炎症病態を担う細胞のため、SLC15A4の機能阻害が他の炎症性疾患にも治療効果をもたらす可能性は高いと考えられます。SLC15A4の阻害剤探索をはじめ、SLC15A4が制御する自然免疫細胞の代謝制御による免疫制御メカニズムの解明をさらに進めることで、今後疾患横断的な治療戦略の作出に大きなブレークスルーをもたらします。